[最も共有された! √] 酸化 化学式 215952-銅 酸化 化学式
酸化銀の熱分解のまとめ 酸化銀の反応前と反応後の物質の性質をまとめると,以下のようになります. 酸化銀の化学式はAg 2 Oなので,銀原子 (Ag)と酸素原子 (O)が含まれています.酸化銀を熱分解すると,なんとなく銀と酸素が出てくると予想できます化学基礎 定期テスト対策酸化還元反応電子を含むイオン反応式 酸化還元反応電子を含むイオン反応式 酸化剤と還元剤との反応で,電子e-を含むイオン反応式のつくり方がよくわかりません。わかりやすく教えてください。 進研ゼミからの回答 こんにちは。いただいた質問について日本大百科全書(ニッポニカ) 酸化クロムの用語解説 クロムと酸素の化合物。クロムの酸化数によってそれぞれ異なる酸化物が知られている。(1)酸化クロム(Ⅱ) 化学式CrO、式量680。クロムアマルガムを空気中に放置すると生ずる黒色粉末で、酸化クロム(Ⅲ)に酸化されやすい。

二氧化氮的化学式怎么书写 星火网校
銅 酸化 化学式
銅 酸化 化学式-(1)は、銅と酸素から酸化銅ができる化学反応式をつくる問題です。 銅酸素→酸化銅 という式がすでに書かれていますね。 まず、銅と酸素と酸化銅をモデルにして描いてみます。 銅はCuで、酸素はOです。また酸化銅はCuOです。Rtecs番号 分子量 化学式 2) 酸化チタン 1558(酸化チ タンとして) 6387 tio 3) 酸化チタン 1558(酸化チ タンとして) xr 7987 tio 2 4) 酸化チタン (アナタース) bv 7987 tio 2 5) 酸化チタン (ルチル) vm 7987 tio 2 6) 三酸化 qチタン 1558(酸化チ タンとして




最新の激安 drager 電気化学式センサー 一酸化炭素 高濃度 ドレーゲルジャパン 株 好評 Learntocaption Com
塩化ナトリウム:NaCl 酸化銅:CuO ) 〇化学反応式→化学変化のようすを化学式を用いて表した式。 ≪例:酸化銀の熱分解≫ ① 化学変化を物質名で表す。 酸化銀 → 銀 + 酸素 ② 物質を化学式で表す。 酸化銅の還元の中学生向け解説ページ です。 「 酸化銅の還元 」 は中学2年生の化学で学習します。 還元とは何か 酸化銅の還元 の実験動画 酸化銅の還元の化学反応式(炭素)まずは、酸化と還元について復習してみましょう。 酸化銅(Ⅱ)と水素の化学反応式は CuO + H 2 → Cu + H 2 O と表せます。
化学反応式 水の電気分解 2H 2 O→2H 2 O 2;(4) 水酸化カルシウム (5) 水酸化バリウム 3次の中和反応を化学反応式で表し,生じた塩の名称を答えよ。 ただし,1:1は物質量の比を示す。この物質量比で反応させたときの化学反応式を書け。 (1)塩酸と水酸化ナトリウム (2)塩酸と水酸化カリウム 水酸化鉄 (ii)を水酸化鉄(iii)にする変化、水酸化鉄(iii)を加熱する変化の化学式(yahoo!japan知恵袋)水溶液中の酸素との反応 4Fe(OH)2 O2 2H2O → 4Fe(OH)3 加熱すると脱水して酸化鉄(Ⅲ)になる 2Fe(OH)3 → Fe2O3 3H2O
塩酸と水酸化ナトリウムの中和 HClNaOH→NaClH 2 O;マグネシウムと塩酸の反応 Mg2HCl→MgCl 2 H2;酸素を用いた定義 酸化 酸化とは物質が酸素と化合することを言います。例えば銅を燃焼させた場合 Cu+O2→2CuO という変化を起こ 例えば銅を燃焼させた場合 Cu+O2→2CuO という変化を起こ



官能团羧酸化学配方结构式 其它png图片素材免费下载 图片编号 Png素材网



酸化還元反応を解説 酸化数を理解して半反応式を覚えよう Studyplus スタディプラス
酸化還元反応式の作り方 半反応式を作る 半反応式を作るには酸化剤、還元剤がどうのように変化するかを覚えていなければならない。 代表的な酸化剤、還元剤は前の"酸化剤と還元剤"にのっているので覚えよう。 作り方は大きく分けて二化学反応式を含め、実験問題及び計算問題ともからむ重要項目ですので、是が非とも内容を理解暗記していきましょう。 今回は酸素と物質(金属)が化合する、「酸化」についてです。 ①銅の酸化 2CuO₂→2CuO ・銅( Cu )十円玉でおなじみの金属。 導線や食器、神社の屋根をふくのに昔から使われてきた金属で、元の色は赤褐色です。 ・酸化銅( CuO )銅粉・「酸化銅を化学式で表せ」 と求められたときも、 読む順番は "うしろが先" だと 知っておくことで、 ・酸化銅 → 銅 + 酸化 → 銅+酸素 → CuO (!) とスムーズに書けます。 理科の「化学式」について、 基本がかなり見えてきましたね!




中2理科 Ght 化学反応式のつくり方 Youtube




Woa1 新規チタン酸モノマーおよびその高分子ならびにその製造方法および用途 Google Patents
水酸化ナトリウム水溶液の電気分解の式では、 「電離式」はnaoh→na()oh() 「化学反応式」は2h(2)o→2ho(2)と教科書に書いてあります。 どちらも同じものなここから4つ(スーパーオキシド、過酸化水素、一重項酸素、ヒドロキシラジカル)の化学式をご説明します。 スーパーオキシド(善玉) 「O」 は酸素原子、 「黄色い 」 は電子化学反応式の例 酸化銀の分解 2Ag 2 O → 4Ag O 2 炭酸水素ナトリウムの分解 2NaHCO 3 → Na 2 CO 3 CO 2 H 2 O 水の分解 2H 2 O → 2H 2 O 2 塩化銅の分解 CuCl 2 → Cu Cl 2 銅の酸化 2Cu O 2 → 2CuO マグネシウムの酸化 2Mg O 2 → 2MgO 炭素の酸化 C O 2 → CO 2 水素の燃焼 2H 2 O 2 → 2H 2 O 鉄と硫黄の化合 Fe S → FeS 銅と塩素の化合 Cu Cl 2 → CuCl 2 銅と硫黄の化合




酸化剤 還元剤で 反応前と反応後の 物質の化学式って覚えるものですか Clearnote
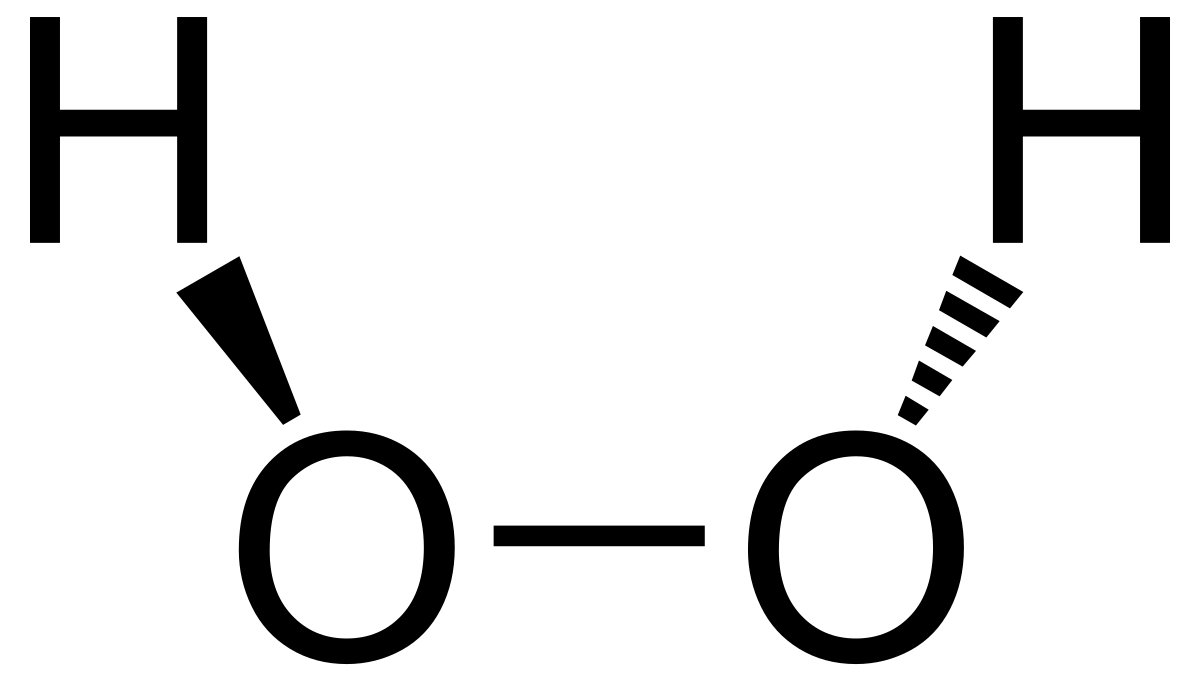



过氧化氢 维基百科 自由的百科全书
赤字がよく出るもの ① 水酸化ナトリウムの電離 NaOH → Na⁺ + OH⁻ ② 水酸化バリウムの電離 Ba(OH)₂ → Ba²⁺ + 2OH⁻ ③ アンモニアが水に溶けたときの電離 NH₃ + H₂O → NH₄⁺ + OH⁻ ④ 水酸化カリウムの電離 KOH → K⁺ + OH⁻化学式で書きなさい。 ⑥物質が酸素と化合する化学変化を何といいますか。 ⑦酸化によってできた物質を何といいますか。 ⑧炭素が酸化してできる物質は何ですか。化学式で書きなさい。 ⑨銅が酸化してできる物質は何ですか。化学式で書きなさい。酸化還元反応式のつくり方 手順1:酸化剤および還元剤の半反応式をつくる。 手順2:2 つ半反応式を連立させて,電子eを消去する。 (酸化還元反応のイオン反応式がここで完成します) 手順3:水素イオンh を,その由来となる適当な酸(h 2so4 など)に置き換える。



勉強のねっこ 理科のねっこ



氯化钠化学式怎么写 初三网
塩化銅の分解 CuCl 2 →CuCl 2;マグネシウムの燃焼 2MgO 2 →2MgO;水素と酸素の化合 2H 2 O 2 →2H 2 O;
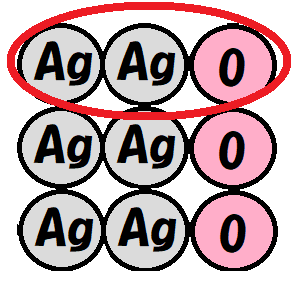



酸化銀のまとめ 中学生用




電離式のつくりかた On Vimeo
この時の化学反応式を考えます。 空気中に置いておいて酸化されてしまうということは、酸素と反応しているということですから 「2Cu2O O2 → 2CuO」 となりますね。化学式nh 4 ohで表される。 しかしこの化学式をもつ化合物は水溶液の中でのみ存在すると,長い間,記述されていたが,アンモニア水の中にこの式に対応する水酸化物の存在することは確認されていない。 また,低温でアンモニア水からnh 3 ・h 2 oの組成をもつ無色六方晶系,融点-7901℃の結晶 なぜ、二酸化ケイ素は分子式ではないんですか? 😭 Clearnote なぜ、二酸化ケイ素は分子式ではないんですか? 😭 b 化学式を示したとき それがの子式である化合物を。 災の0 6のうちから一つ選べ ⑩ 者化ナトリゥム @ 酸化アルミニッウム @ 塩化水素 ⑳
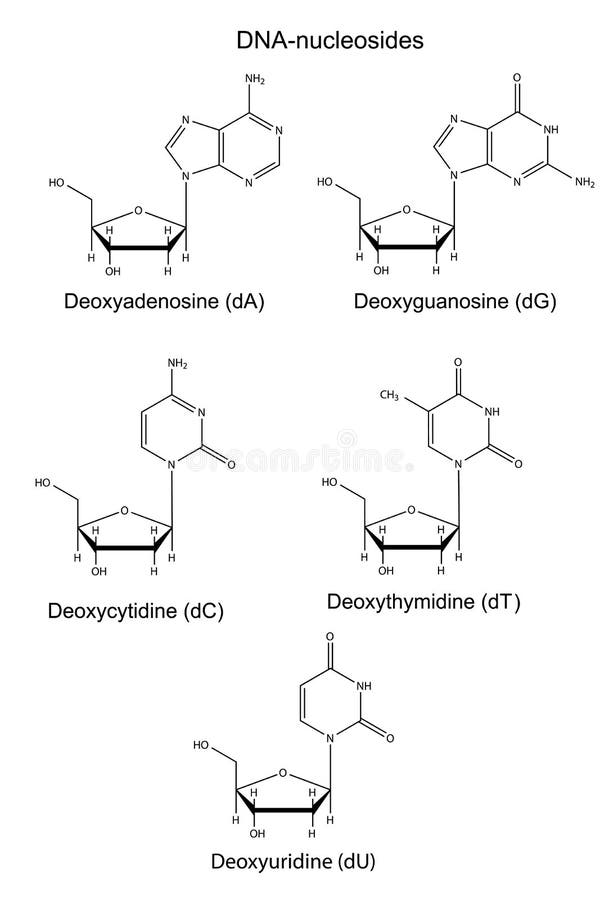



脱氧核糖核酸核苷结构化学式向量例证 插画包括有生物 部门 大分子 酸化 双眼 有机 设计




最新 酸化 化学式 りんご 酸化 化学式
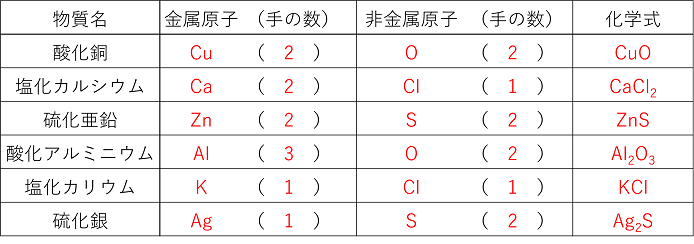
「化学式」とは、 ある物質の成り立ちを原子の記号と数字で表した式 のことをいいます。 「原子の記号」は「 元素記号 」とも呼ばれ、酸素や水素などをアルファベットで表します。 化学反応式10非金属の酸化反応 \c o_{2} → co_{2}\\ 2h_{2} o_{2} → 2h_{2}o \ この反応は酸化数を考えると酸化還元反応であることが分かりやすい。 炭素cは単体なので酸化数0なのに対して、反応後の二酸化炭素co 2 に含まれるcの酸化数は+4。したがって、酸化数が増加してる鉄に見られる錆の種類と成分、化学式の一覧 以下、鉄や鉄鋼が腐食した際にできる錆の種類ごとの特徴と、錆の成分と化学式について見ていきます。 水酸化鉄 鉄や鋼においては、最初にできる錆がこの水酸化鉄のうち、水酸化第一鉄です。初期は白色や




氢氧化钠 维基百科 自由的百科全书



化学式 物質の密度
関連:計算ドリル、作りました。 半反応式の作り方 step1 酸化剤(還元剤)が何 銅+酸素→酸化銅 これを化学式を使って書き換える。 Cu+O2→CuO 左辺と右辺で銅と酸素の原子の数を確認する。銅は1個ずつで合っているが、酸素は左辺が2個で右辺は1個。 個数の少ないほうを多い方と同じになるように変形する。右辺を2倍して、 Cu+O2→2CuO このとき、2倍した2は化学式の前「水素 + 酸素 → 水」の式をそのまま化学反応式に直すと「h2 o2 →h2o」になりますが、両辺のHとOの数を数えてみて下さい。 左にはHが2個、Oが2個なのに、右にはHが2個の、Oが1個しかありま
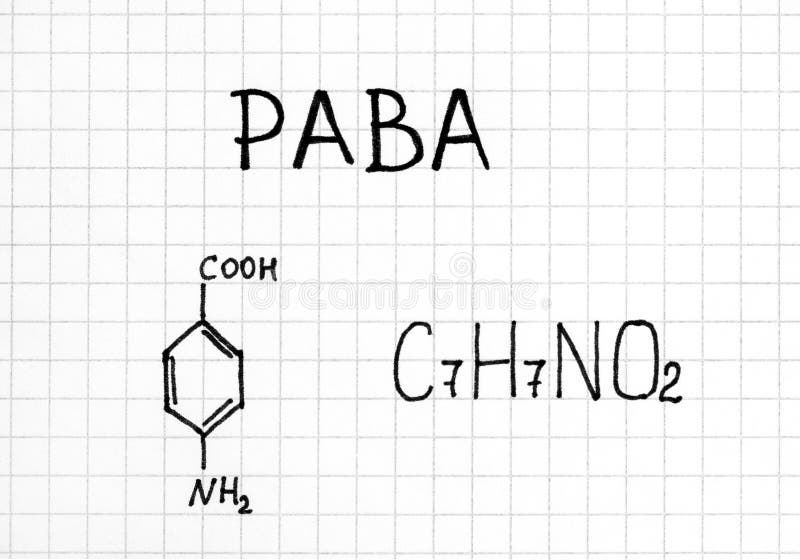



Paba化学式库存照片 图片包括有没人 结构 酸化 学习 科学 教育 化学 化学制品
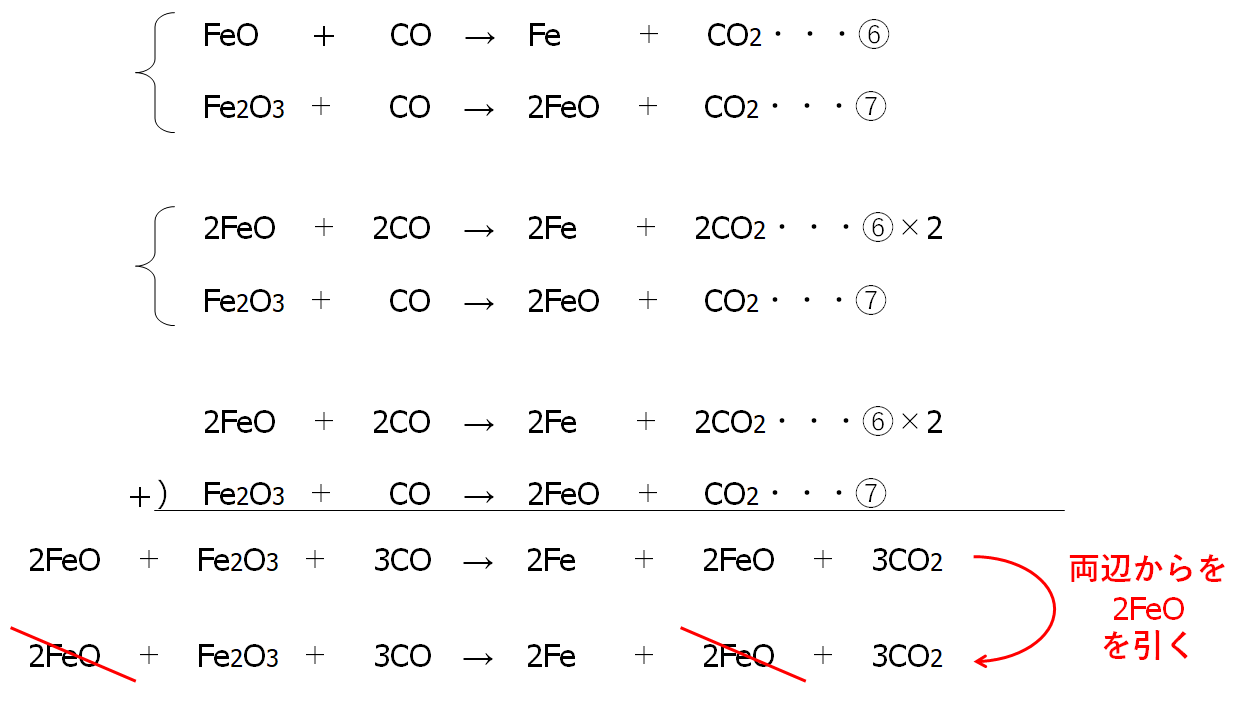



中2化学 鉄の精錬 中学理科 ポイントまとめと整理




检验氯离子要加入的试剂 硝酸酸化的硝酸银溶液 硝酸银检验氯离子




Vova Household Carbon Monoxide Alarm Co Alarm Co Sensor Monitor Prevent Fire Carbon Monoxide Poisoning




58 酸化物の化学式 ニューグローバル解いてみた Youtube




高考化学压轴笔记 新课标版 加分点全在这 知乎




一酸化炭素 Co の化学式 分子式 構造式 電子式 イオン式 分子量は 炭素の不完全燃焼の反応式は



无色酚酞化学式 扒拉扒拉




なぜ 酸化銀の化学式は2agoでなく Ag2oなのですか Clearnote
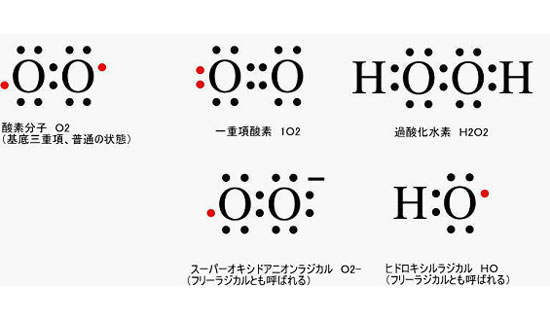



活性酸素とは構成する電子が不安定になった酸素 細胞膜やdnaなどが酸化し老化現象を引き起こします




一点就通的高中化学 5类难写化学方程式归纳 总结 考前短时间就能掌握噢 哔哩哔哩
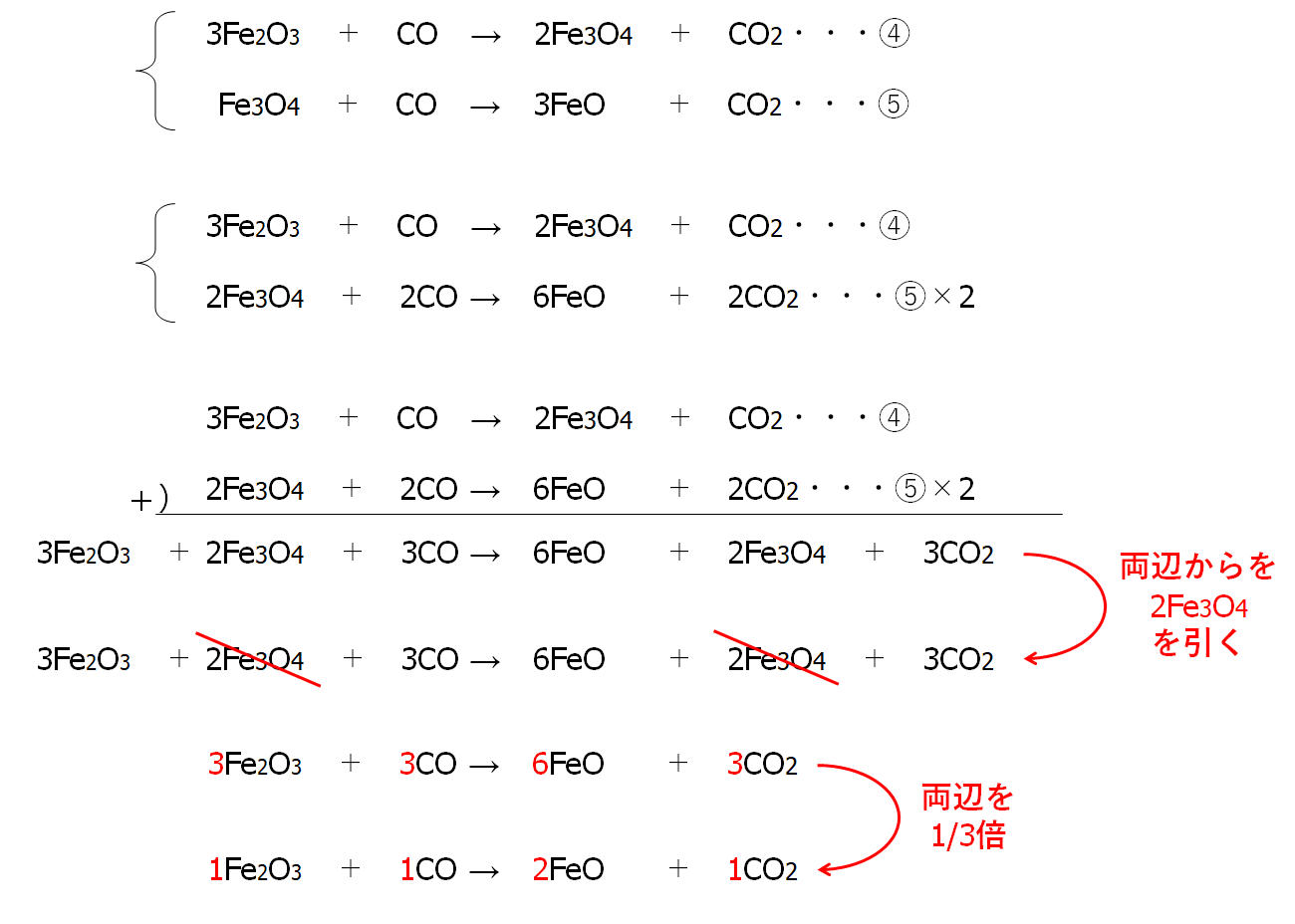



中2化学 鉄の精錬 中学理科 ポイントまとめと整理




なぜ 酸化銀の化学式はagに2が付くのですか Clearnote




下の図のように 酸化銀の化学式は Ag2o ですが 化学反応式では Clearnote



乙酸化学结构式羧酸氨基酸png图片素材免费下载 图片编号 Png素材网




7 Tips To Help You Maintain Healthy Teeth Wikitionary254




一酸化炭素 Co の化学式 分子式 構造式 電子式 イオン式 分子量は 炭素の不完全燃焼の反応式は
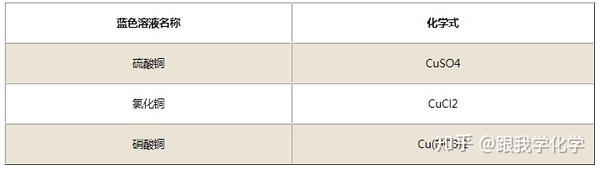



初中蓝色溶液有哪些蓝色溶液的化学式 知乎
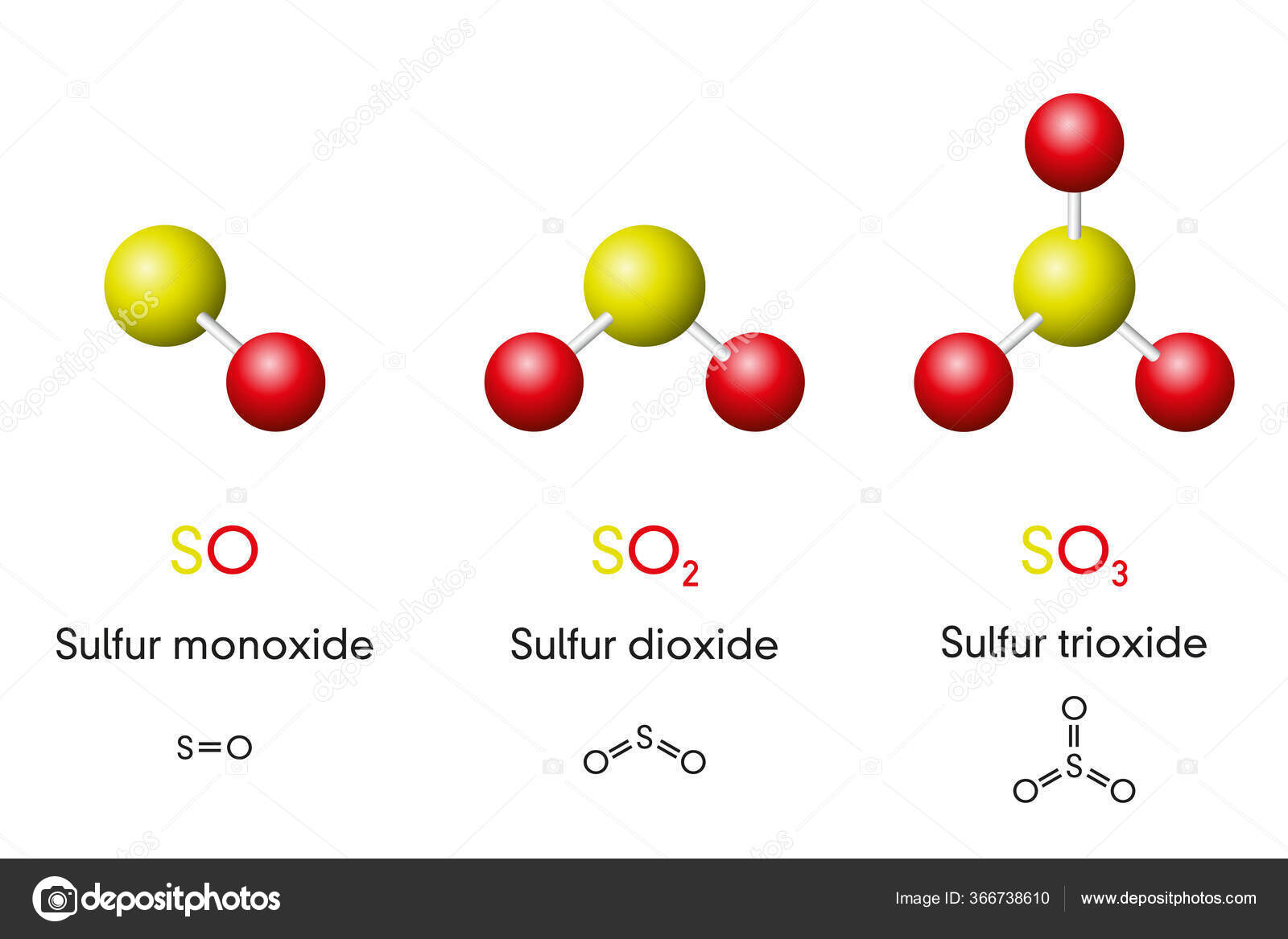



Three Sulfur Oxides Molecule Models Chemical Formulas Sulfur Monoxide Dioxide Stock Vector Image By C Furian



着色酸化剤組成物




51 2 Aluminium Hydroxide Gel 012 Detail Information Life Science Laboratory Chemicals Fujifilm Wako Chemicals U S A Corporation




酸化数とは 求め方 計算問題 理系ラボ



Antimony Oxide Sb2o3 Mixed With Arsenic Oxide As2o3 Cas 651 38 2
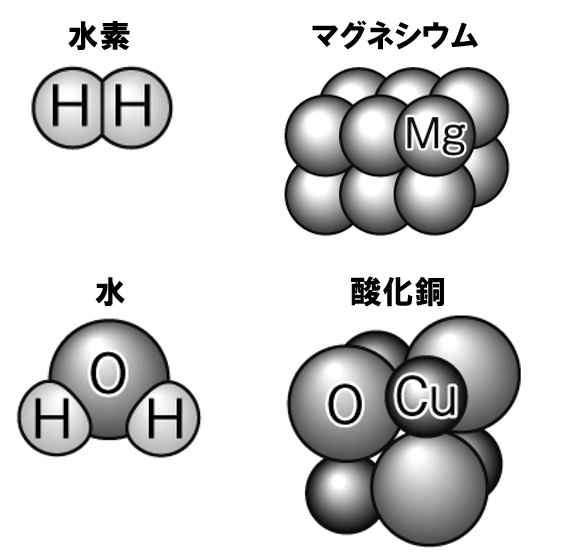



中2理科問題 原子の記号 化学式の暗記用問題 Examee



最新 酸化 化学式 りんご 酸化 化学式
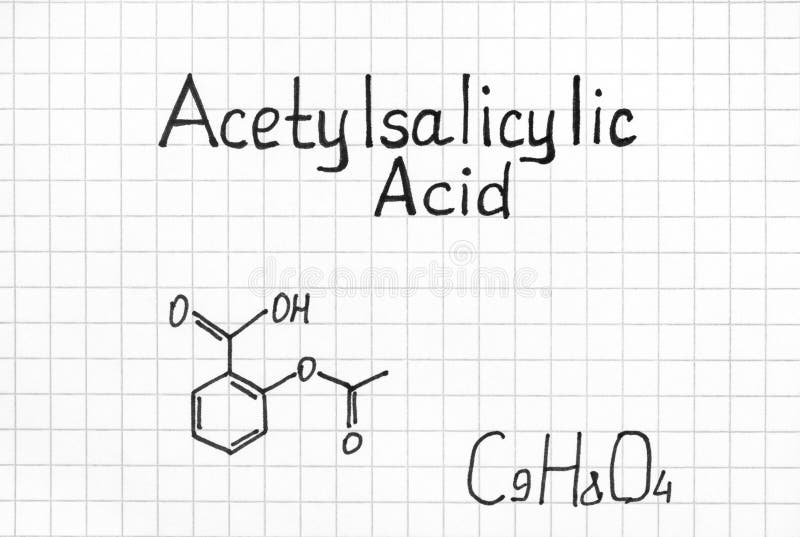



乙酰水杨酸化学式库存图片 图片包括有酸化 分子 文字 纸张 研究 手写 技术 学习



氯化钠cas 氯化钠的化学式是什么 治工网
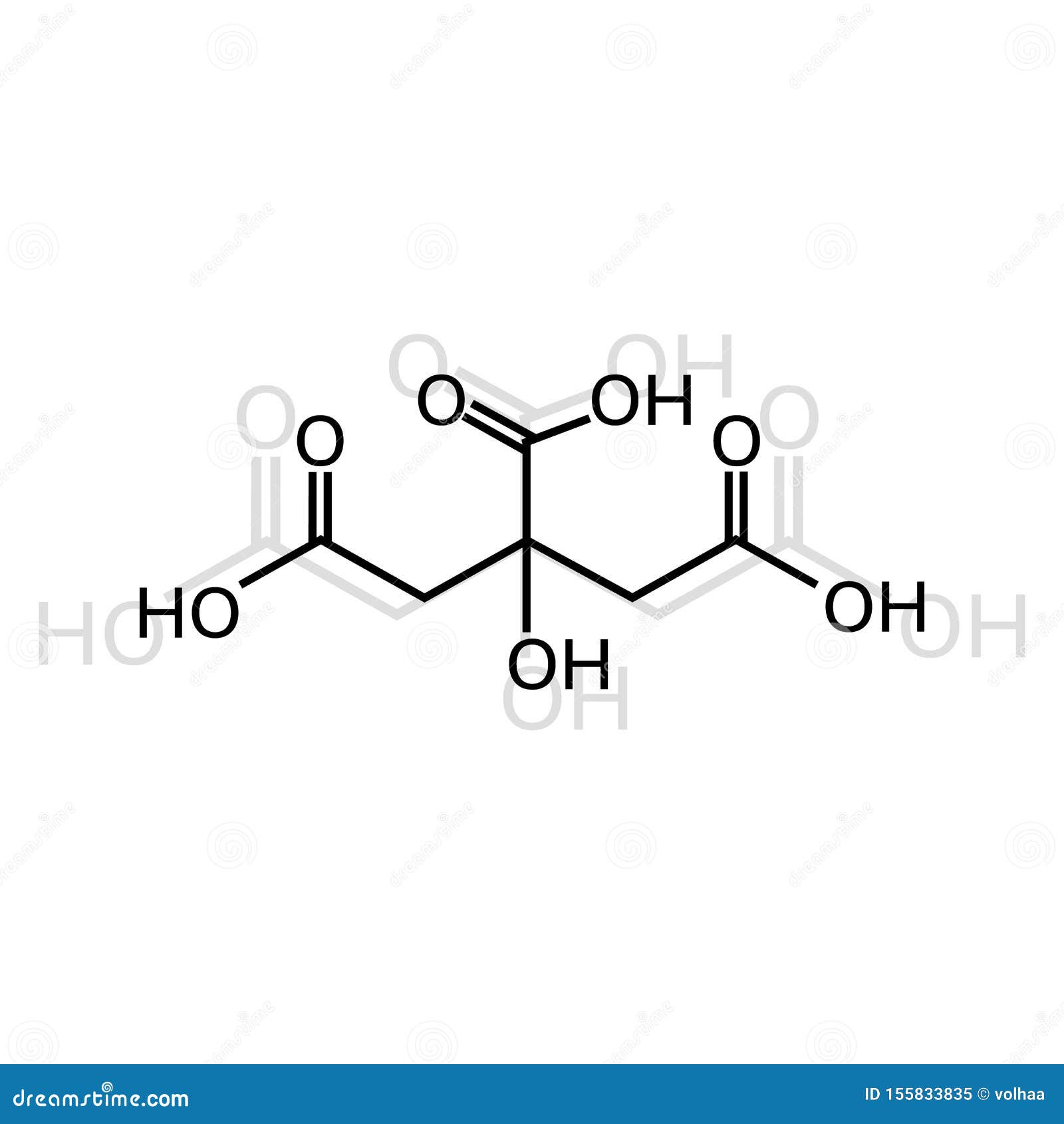



柠檬酸化学式向量例证 插画包括有酸化 空白 影子 结构 配方 背包 柠檬 柠檬酸




ファイル Redox Cuo Chemical Formula Jp Svg Wikibooks




Woa1 油性インクを用いた印刷方法および油性インク用記録用紙 Google Patents




酸化銀の化学式ag2oのモデルが分かりません Clearnote
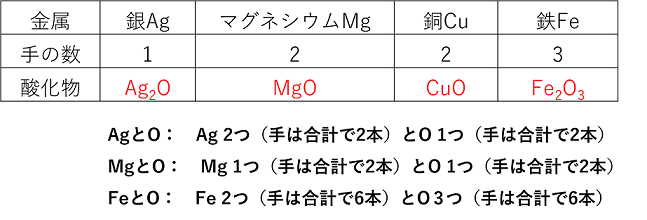



物質の酸化



Iyg0p6ffig94m




一酸化炭素と二酸化炭素の分子化学式 二酸化炭素のベクターアート素材や画像を多数ご用意 Istock



化学式练习




高1の化学です 酸化された物質を化学式で答えよ という問題です 高校 教えて Goo




覚えておきたい化学式一覧 Hiromaru Note



酸雨的主要成分化学式是什么 初三网




二氧化铼 维基百科 自由的百科全书



71 6 Barium Hydroxide Octahydrate 026 0 024 Detail Information Common Chemicals Lab Tools Laboratory Chemicals Fujifilm Wako Chemicals Europe Gmbh




最新の激安 drager 電気化学式センサー 一酸化炭素 高濃度 ドレーゲルジャパン 株 好評 Learntocaption Com
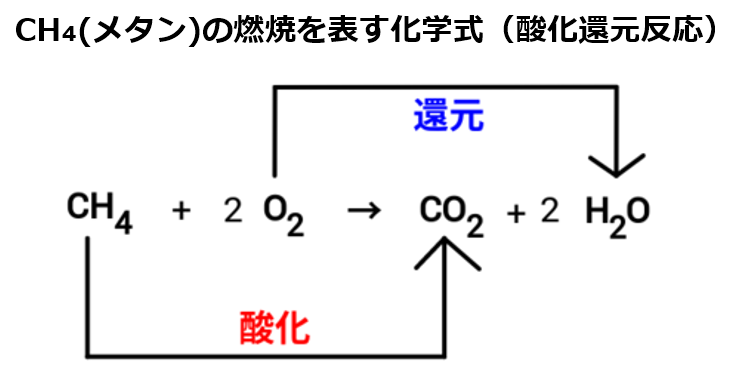



酸化還元反応 電子のやり取り




二氧化氮的化学式怎么书写 星火网校



柠檬酸化学式向量例证 插画包括有酸化 空白 影子 结构 配方 背包 柠檬 柠檬酸




二酸化窒素は化学式の No2 を化合物です いくつかの窒素酸化物の一つです No2 は硝酸の工業合成の中間体です 3 D イラストレーション の写真素材 画像素材 Image



氧化铁黄 化学式为feooh 是一种黄色颜料 工业上用废铁为主要原料生产氧化铁黄的一种工艺流程如图1 1 废铁在反应前常用热的纯碱溶液清洗表面油污 其原理是 写离子方程式 立事作业互答平台 专业的学生作业问答网站



酸化ニッケル Iii Wikipedia



化学式の質問です理科のテキストで酸化銅の化学式が2cu O2 2cuoと解 Yahoo 知恵袋




一酸化炭素 コロラド州分子モデルと化学式 一酸化炭素のベクターアート素材や画像を多数ご用意 Istock




中2理科 銅 酸素の化学反応式 練習編1 映像授業のtry It トライイット




化学式练习




酸化カリウム Wikipedia




化学式 塾の質問箱
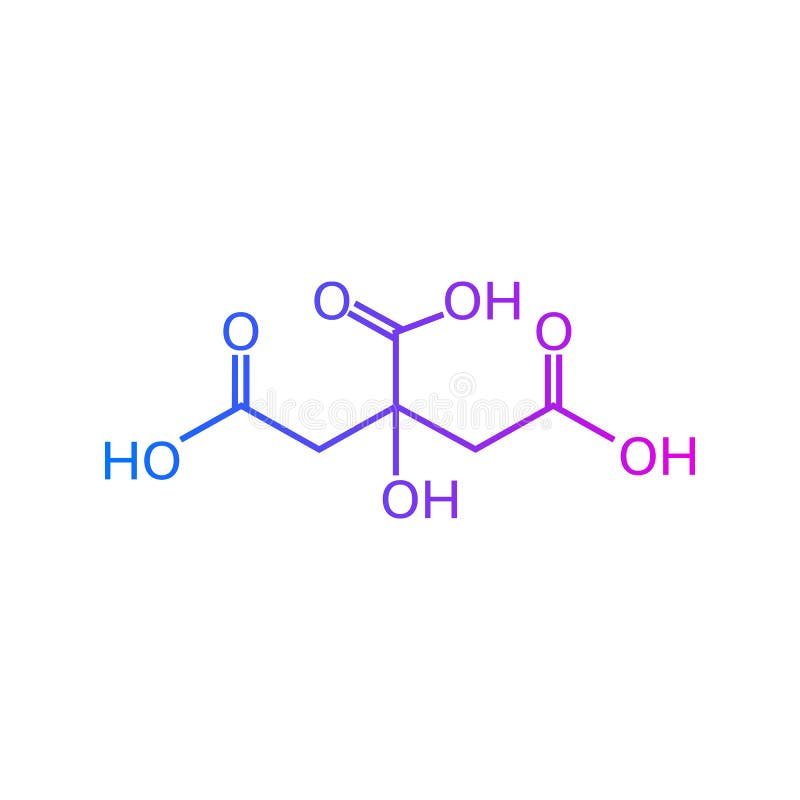



柠檬酸化学式向量例证 插画包括有背包 酸化 结构 梯度 柠檬 图标 配方 空白 化学
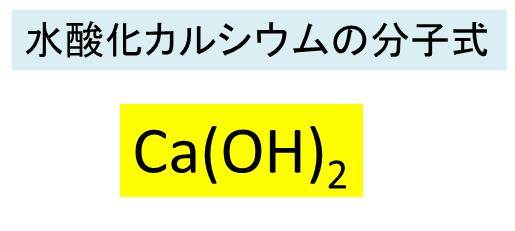



水酸化カルシウム Ca Oh 2 の化学式 組成式 構造式 電子式 分子量は 水酸化カルシウム 石灰水 と二酸化炭素との反応式は
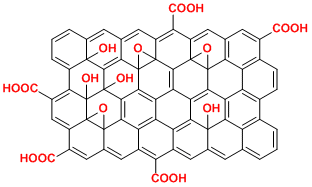



Graphene Oxide Tci Europe N V




臺灣記憶taiwan Memory
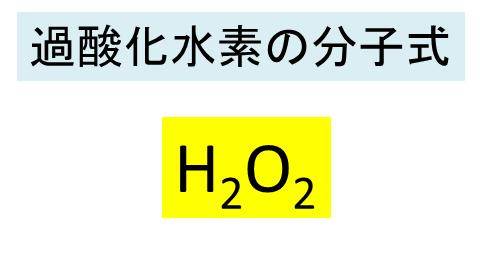



過酸化水素 H2o2 の化学式 分子式 構造式 電子式 分子量は 過酸化水素の分解の反応式は



西村貴之 1vr3pv6x9wvnytf Twitter



次氯酸化学式 万图壁纸网




どうやってどの化学式を酸化数を求めればよいのか分かるのですか 至急お願いします Clear



十酸化四リン You Iggy




硝酸酸化的硝酸银溶液是什么意思 解历史
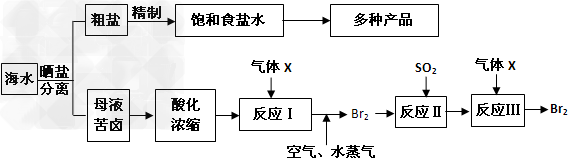



1 A为用惰性电极电解饱和食盐水 含少量ca2 Mg2 的装置 电解一段时间后 B中出现浑浊现象 请用离子方程式表示原因 新东方在线网络课堂



化学式练习




理科 中2 7 化学反応式の作り方 Youtube



酸化還元反応で酸化されたか還元されたか答える問題でなぜやじるしのむきに Yahoo 知恵袋
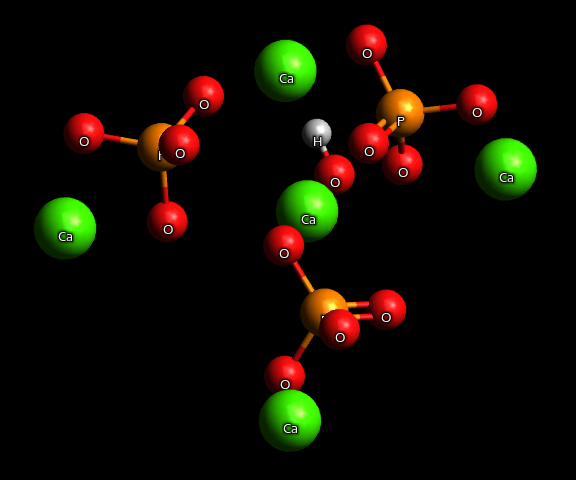



File Hydroxylapatit Auch Hydroxyapatit Apatit Caoh Dargestellt Von Avogadro Png Wikimedia Commons




化学式练习



Hpo42 是什么离子 扒拉扒拉
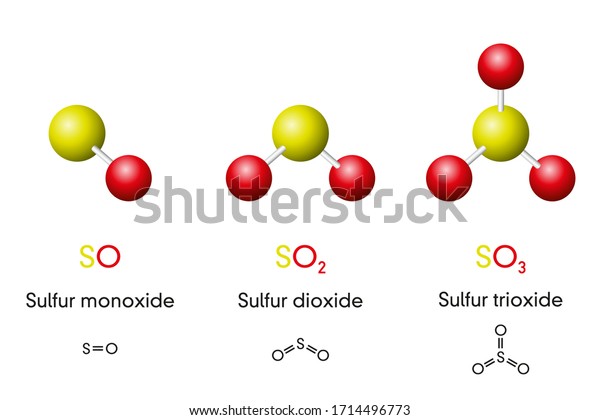



Three Sulfur Oxides Molecule Models Chemical Stock Vector Royalty Free



化学式 6 について 酸化マンガン について マンガンの Yahoo 知恵袋



蒽酸化学式分子式化合物 化合物png图片素材免费下载 图片编号 Png素材网




氧化鈣 维基百科 自由的百科全书



酸化鉄 Ii Iii You Iggy




化学式 Wikiwand



酸化銀の化 6 式ってこれであ 照片共享页面 撮影蔵




中3化学 化学式の作り方 知識問題 中学理科の問題パターンと練習問題




最新 酸化 化学式 りんご 酸化 化学式




化学反応式 Ict教材eboard イーボード




宇宙一覚えやすい 化学反応式ハンドブック Amazon Com Books



氯化钠的化学式是什么氯化钠的化学式正确写法



化学式练习



次氯酸化学式 万图壁纸网




酸化鉛 の化学式がpbo になる理由が分かりません Clearnote



醋酸的化学式 初三网
コメント
コメントを投稿